主要行业
点击进入可选择细分行业
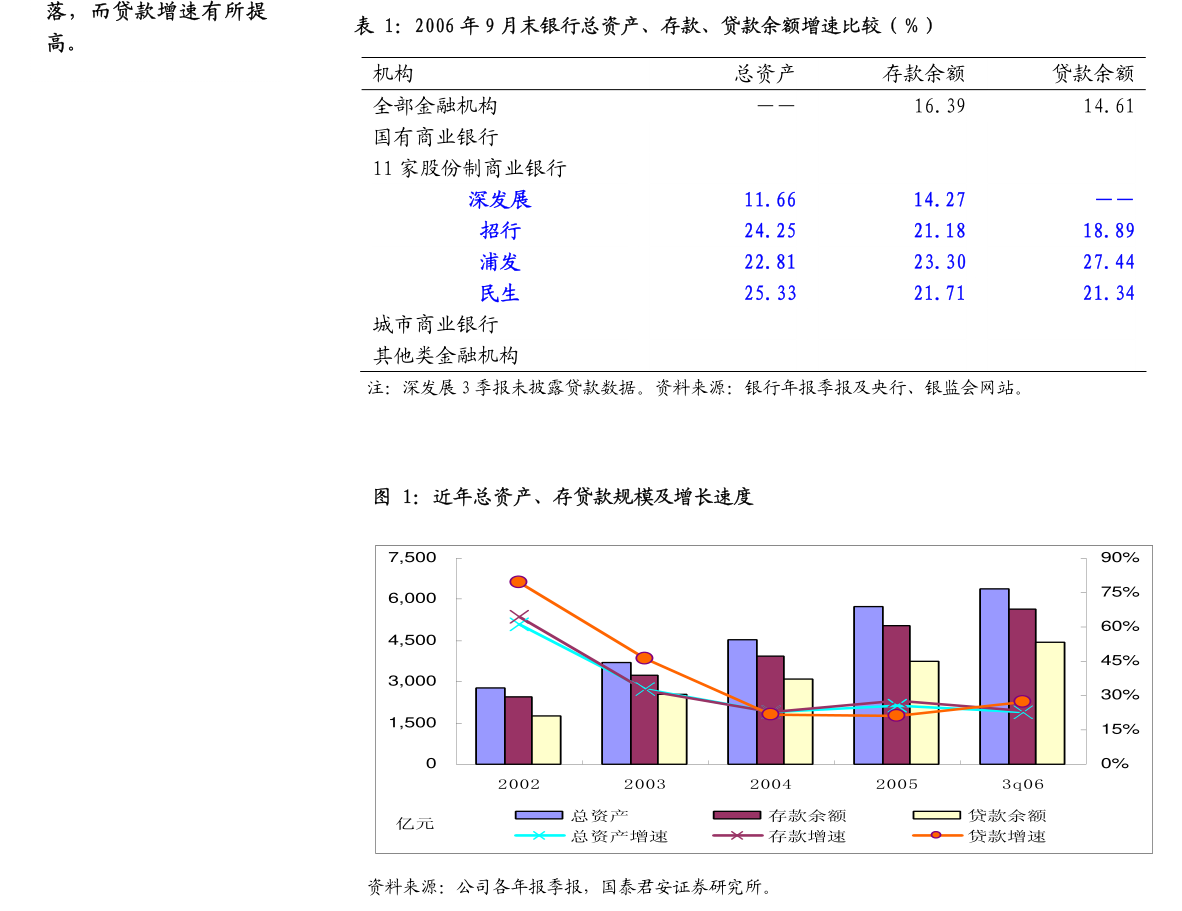
1. 1香港交易及結算所有限公司及香港聯合交易所有限公司對本公告的內容概不負責,對其準確性或完整性亦不發表任何聲明,並明確表示,概不對因本公告全部或任何部份內容而產生或因倚賴該等內容而引致的任何損失承擔任何責任。
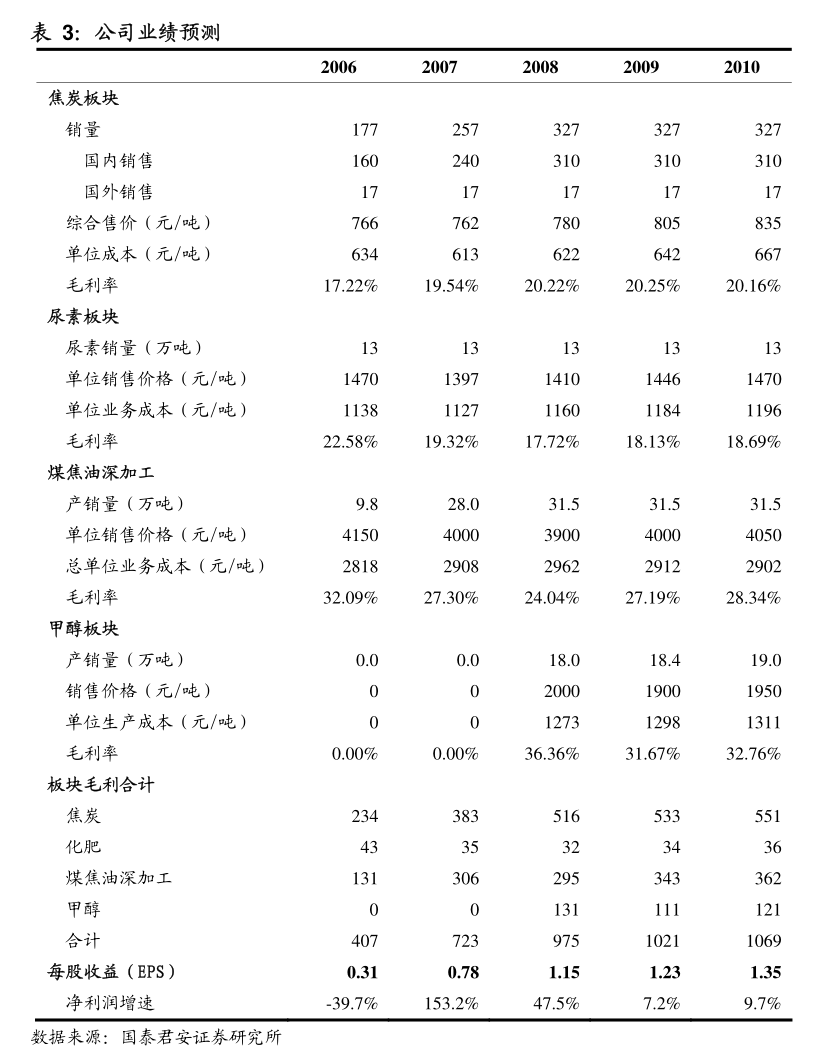
2. SichuanKelun-BiotechBiopharmaceuticalCo.,Ltd.四川科倫博泰生物醫藥股份有限公司(於中華人民共和國註冊成立的股份有限公司)(股份代號:6990)自願公告核心產品蘆康沙妥珠單抗(sac-TMT)於2024年美國臨床腫瘤學會年會上公佈的研究成果四川科倫博泰生物醫藥股份有限公司(「本公司」)董事(「董事」)會(「董事會」)欣然宣佈,本公司將在於2024年5月31日至6月4日於美利堅合眾國伊利諾伊州芝加哥市舉行的2024年美國臨床腫瘤學會(ASCO)年會上,於當地時間2024年6月2日早上9:45至11:15舉辦的臨床科學研討會(摘要#104;下一代抗體藥物偶聯物:變革在繼續)上公佈其抗TROP2ADC蘆康沙妥珠單抗(sac-TMT)(前稱SKB264/MK-2870)用於既往接受過治療的局部復發或轉移性三陰性乳腺癌(TNBC)患者的3期研究(OptiTROP-Breast01)結果。
3. 此外,於當地時間2024年5月31日下午2:45至5:45的口頭報告環節(摘要#8502;肺癌-轉移性非小細胞),本公司將展示蘆康沙妥珠單抗(sac-TMT)聯合KL-A167(抗PD-L1單抗)用於一線治療晚期非小細胞肺癌(NSCLC)患者的2期研究(OptiTROP-Lung01)結果。
4. 蘆康沙妥珠單抗(sac-TMT)在臨床階段為本公司與默沙東(美國新澤西州羅威市默克公司的商號)聯合開發。
5. 上述研究摘要已於當地時間2024年5月23日發佈於ASCO的官方網站上。
6. 研究成果概述如下:TNBC患者按1:1隨機接受蘆康沙妥珠單抗(sac-TMT)治療(n=130)或化療(n=133)。

7. 患者中位年齡為51歲;87%存在內臟轉移;26%既往接受過PD-1/PD-L1抑製劑治療;48%在晚期階段接受過三線或以上的化療。
8. 根據期中分析(數據截止日期:2023年6月21日),已達到無進展生存期(PFS)主要終點,相比化療,疾病進展或死亡的風險降低69%(風險比(HR):0.31;95%置信區間(CI):0.22至0.45;P<0.00001)。
9. 2根據BICR評估,蘆康沙妥珠單抗(sac-TMT)的中位PFS為5.7個月(95%CI:4.3至7.2),化療的中位PFS為2.3個月(95%CI:1.6至2.7),6個月的PFS率分別為43.4%/11.1%。
10. 在滋養層細胞表面抗原2(TROP2)H評分>200的患者亞組中,蘆康沙妥珠單抗(sac-TMT)的中位PFS為5.8個月,化療的中位PFS為1.9個月(HR:0.28;95%CI:0.17至0.48)。
11. 在總生存期(OS)的首次計劃期中分析中(數據截止日期:2023年11月30日,中位隨訪時間10.4個月),相比化療,蘆康沙妥珠單抗(sac-TMT)的OS顯示出具有統計學意義的顯著優勢(HR:0.53;95%CI:0.36至0.78;P=0.0005);蘆康沙妥珠單抗(sac-TMT)的中位OS尚未達到(95%CI:11.2至NE),而化療的中位OS為9.4個月(95%CI:8.5至11.7)。
12. 基於BICR評估,蘆康沙妥珠單抗(sac-TMT)的客觀緩解率(ORR)為43.8%,化療的ORR為12.8%。
13. 最常見的≥3級治療相關不良事件(TRAE)(蘆康沙妥珠單抗(sac-TMT)/化療)為中性粒細胞計數降低(32.3%/47.0%)、貧血(27.7%/6.1%)及白細胞計數(WBC)降低(25.4%/36.4%)。
14. 默沙東主導的一項評估蘆康沙妥珠單抗(sac-TMT)聯合帕博利珠單抗對比研究者選擇方案(TPC)治療既往接受過新輔助治療且在手術時未達到病理學完全緩解(pCR)的TNBC患者的3期全球研究(NCT06393374),及本公司主導的一項評估蘆康沙妥珠單抗(sac-TMT)在中國用於一線治療不可手術切除的局部晚期、復發或轉移性PD-L1陰性TNBC患者的3期研究(NCT06279364)正在進行中。
15. NSCLC未曾接受過治療的晚期無驅動基因突變NSCLC患者入組並按非隨機方式每3週接受一次5mg/kg劑量的蘆康沙妥珠單抗(sac-TMT)加每3週接受一次1200mg劑量的KL-A167治療(1A隊列)或每2週接受一次5mg/kg劑量的蘆康沙妥珠單抗(sac-TMT)加每2週接受一次900mg劑量的KL-A167治療(1B隊列),直至疾病進展或發生不可耐受毒性。
16. 截至2024年1月2日,1A隊列和1B隊列分別入組40名及63名患者。
中位年齡為63/63歲(1A/1B隊列);97.5%/85.7%患者的美國東部腫瘤協作組體能狀態(ECOGPS)評分為1分;根據IHC22C3pharmDx測定法,分別有30.0%/33.3%、32.5%/30.2%及37.5%/36.5%的患者腫瘤細胞的程式性死亡配體1(PD-L1)表達為<1%、1%-49%及≥50%。
31A隊列經過為期14.0個月的中位隨訪後,ORR為48.6%(18/37,2例待確認),疾病控制率(DCR)為94.6%,中位PFS為15.4個月(95%CI:6.7,NE),6個月PFS率為69.2%。
1B隊列經過為期6.9個月的中位隨訪後,ORR為77.6%(45/58,5例待確認),DCR為100%,未達到中位PFS,6個月的中位PFS率為84.6%。
1B隊列的其他亞組分析如下表所示:ORR,%(n/N)*6個月PFS率,%(95%CI)總體人群(N=63)77.6(45/58)84.6(71.4,92.1)組織學類型非鱗狀(N=34)72.7(24/33)93.8(77.3,98.4)鱗狀(N=29)84.0(21/25)73.5(49.9,87.2)PD-L1TPS<1%(N=21)63.2(12/19)82.2(54.3,93.9)1%-49%(N=19)81.3(13/16)76.6(41.2,92.3)≥50%(N=23)87.0(20/23)91.3(69.5,97.8)*包括已確認或尚未確認緩解。
ORR基於有療效評估的患者計算(定義為在研究期間進行過至少1次掃描)。
在1A和1B隊列中,最常見的≥3級TRAE為中性粒細胞計數降低(30.0%/30.2%)、WBC降低(5.0%/17.5%)、貧血(5.0%/15.9%)、皮疹(5.0%/6.3%)及藥疹(7.5%/0)。
曾發生1B隊列的1名患者因出現超敏反應導致停用蘆康沙妥珠單抗(sac-TMT)的治療相關不良事件,但並無出現治療相關死亡事件。
目前兩項由默沙東主導的蘆康沙妥珠單抗(sac-TMT)用於3L+EGFR突變NSCLC患者(NCT06074588)及2LEGFR突變NSCLC患者(NCT06305754)的全球3期研究,以及一項由本公司主導的在中國開展的用於2LEGFR突變NSCLC患者的3期研究(NCT05870319)正在進行中。
此外,三項由默沙東主導的蘆康沙妥珠單抗(sac-TMT)聯合帕博利珠單抗的全球3期研究也正在進行中:一項是用於一線治療轉移性鱗狀NSCLC患者(NCT06422143),第二項是用於PD-L1表達≥50%的轉移性NSCLC患者(NCT06170788);第三項是用於未獲得病理完全緩解的可切除NSCLC患者(NCT06312137)。
4風險警告蘆康沙妥珠單抗(sac-TMT)最終不一定能夠成功開發及商業化。
本公司股東及潛在投資者於買賣本公司證券時務請審慎行事。
承董事會命四川科倫博泰生物醫藥股份有限公司董事長兼非執行董事劉革新香港,2024年5月24日於本公告日期,董事會包括董事長兼非執行董事劉革新先生;執行董事葛均友博士及王晶翼博士;非執行董事劉思川先生、馮昊先生、曾學波先生及李東方先生;及獨立非執行董事鄭強博士、涂文偉博士、金錦萍博士及李越冬博士。

正在加载,请稍候...