
1. 1香港交易及結算所有限公司及香港聯合交易所有限公司對本公告之內容概不負責,對其準確性或完整性亦不發表任何聲明,並明確表示,概不就因本公告之全部或任何部分內容而產生或因倚賴該等內容而引致之任何損失承擔任何責任。
2. JiangsuRecbioTechnologyCo.,Ltd.江蘇瑞科生物技術股份有限公司(於中華人民共和國註冊成立的股份有限公司)(股份代號:2179)自願公告重組九價HPV疫苗III期臨床試驗進展本公告由江蘇瑞科生物技術股份有限公司(「本公司」,連同其附屬公司,統稱為「本集團」)自願作出。

3. 本公司董事會(「董事會」)欣然宣佈,本公司已於近日完成其重組九價HPV疫苗REC603(「REC603」)的小年齡組免疫橋接、及與Gardasil9免疫原性比較兩項研究的全部受試者入組和首劑接種工作。
4. 同時,REC603主效力試驗的受試者正在按照臨床方案開展隨訪工作。
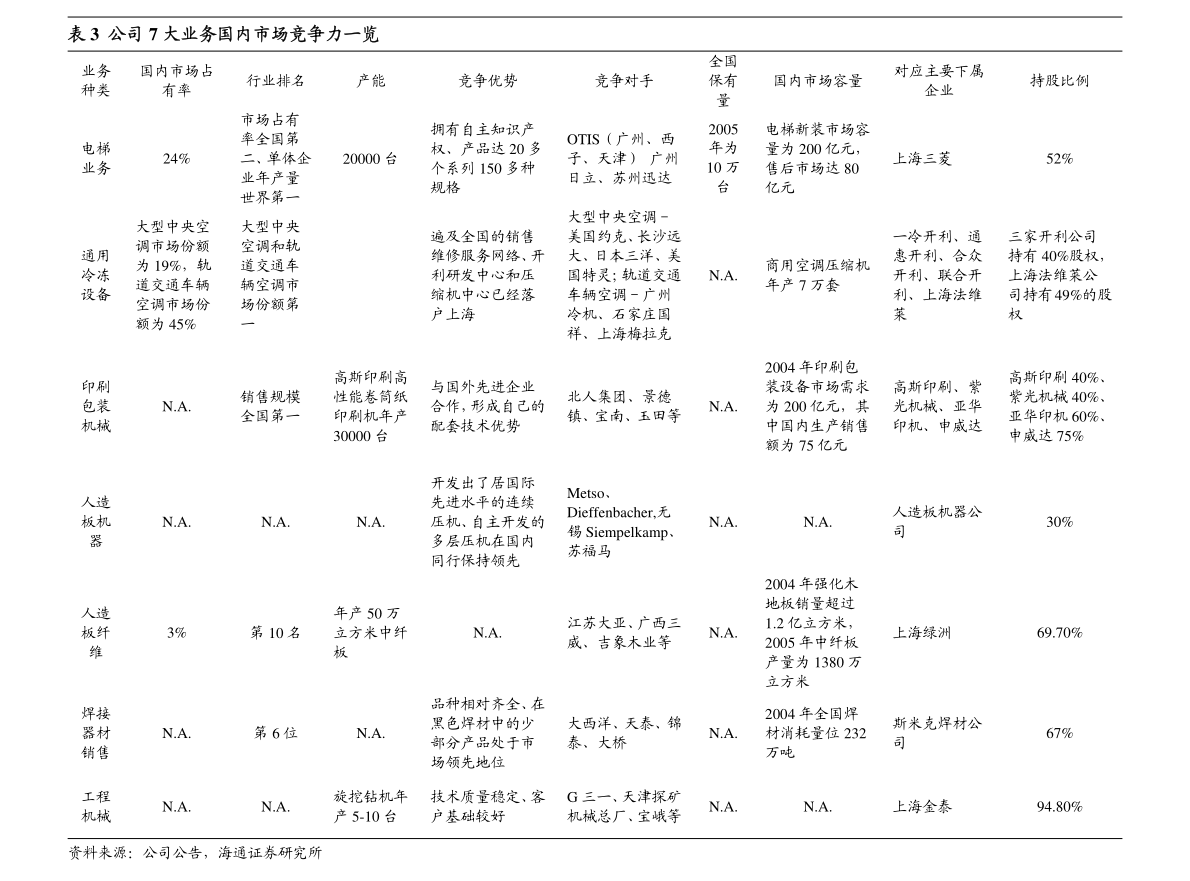
5. REC603中國III期臨床試驗由主效力試驗、小年齡組免疫橋接試驗、與Gardasil9免疫原性比較試驗三部分組成,採用多中心、隨機、盲態、平行對照設計,受試者總樣本量為16,050例:主效力試驗:在18-45歲健康女性中,評價試驗疫苗所含HPV高危型別感染相關的高級別宮頸、外陰、陰道高級別上皮內瘤樣變及以上病變的保護效力為主要有效性終點小年齡組免疫橋接試驗:評價9-17歲健康女性全程接種試驗疫苗後1個月時血清中和抗體相較於18-45歲健康女性的非劣效性與Gardasil9免疫原性比較試驗:在16-26歲健康女性中,評價全程接種試驗疫苗後1個月時血清中和抗體相較於Gardasil9的非劣效性2九價HPV疫苗可預防約90%的宮頸癌及90%的肛門及生殖器疣,被廣泛認為是針對HPV的最有效疫苗。
6. 目前,尚無國產九價HPV疫苗獲批在中國銷售。
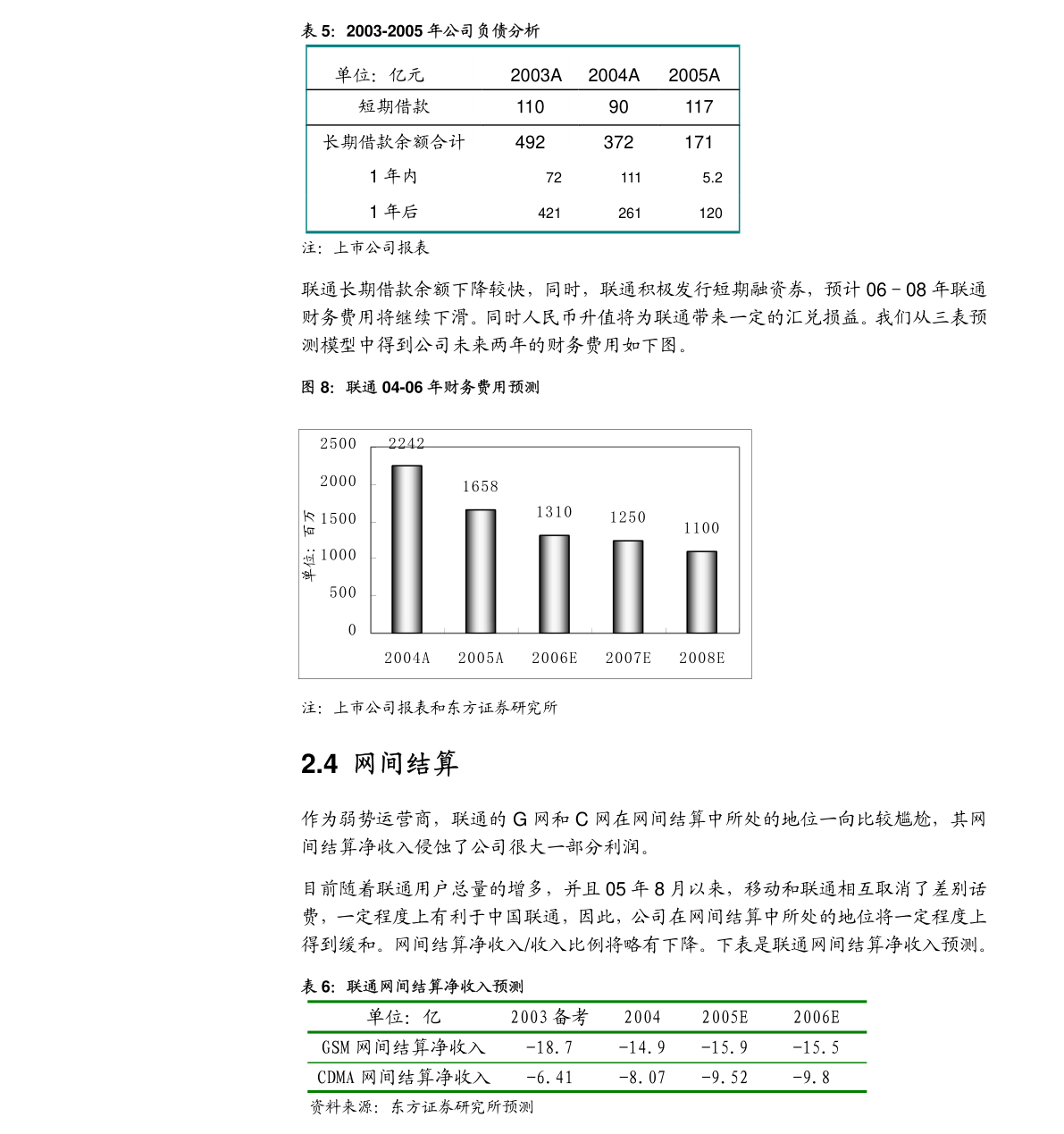
7. 已完成的I期臨床數據顯示,REC603安全且耐受,具有良好的免疫原性。
8. REC603採用漢遜酵母表達系統,實現了HPV病毒樣顆粒的高產及穩定表達,使本公司的候選疫苗更適合作商業化生產。
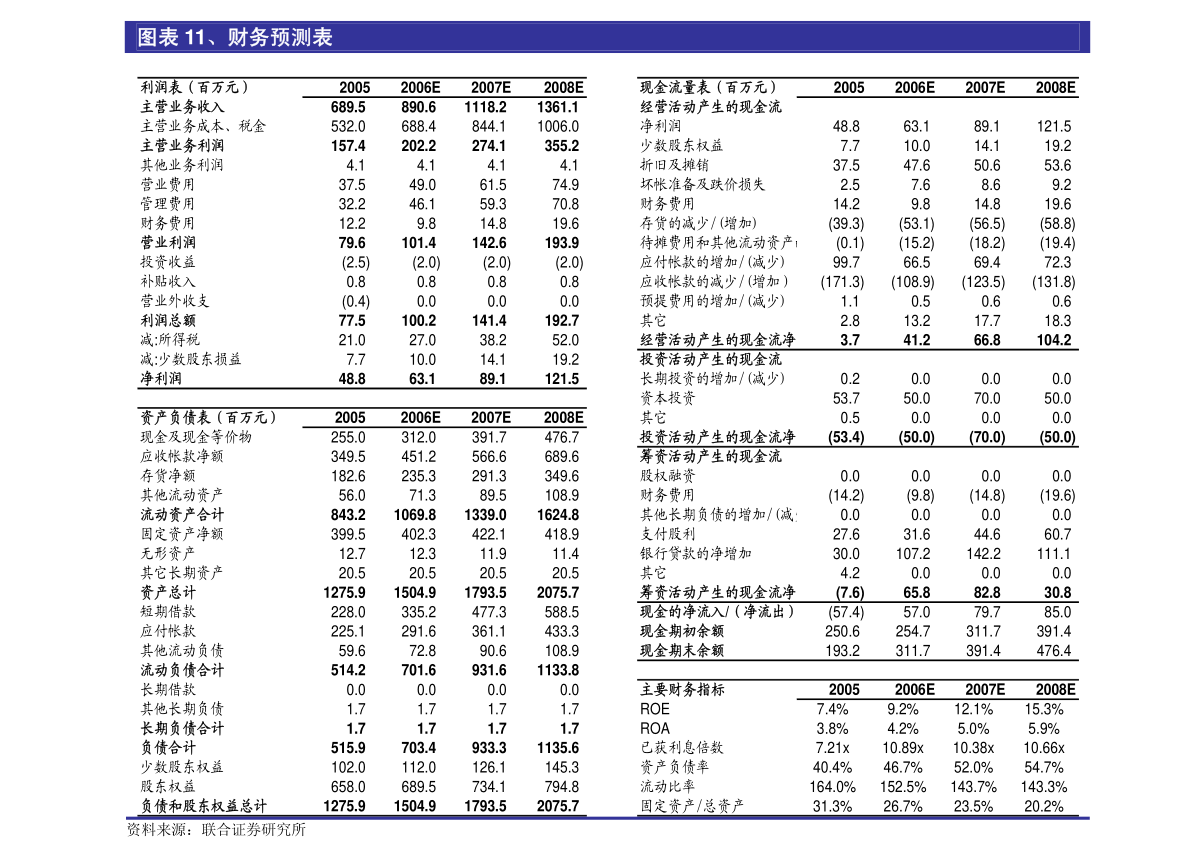
9. 憑藉明確的關鍵工藝參數及控制策略,REC603易於擴展生產規模,以滿足國內及全球市場的需求。
10. 股東及潛在投資者應注意,本集團未必能成功開發或營銷REC603,於買賣本公司證券時務請審慎行事。

11. 承董事會命江蘇瑞科生物技術股份有限公司主席劉勇博士中國江蘇省,2022年8月9日於本公告日期,董事會包括董事會主席兼執行董事劉勇博士,執行董事陳健平博士及李布先生,非執行董事洪坤學博士、周宏斌博士、趙輝先生、杜威博士及逢濤博士,以及獨立非執行董事梁國棟先生、夏立軍博士、GAOFeng教授及袁銘輝教授。









